Нобелевскую премию по химии 2021 года присудили за довольно маленькие молекулы. Причем некоторые из них совсем не новые — аминокислоту пролин, например, открыли еще в 1900 году. Но прелесть их не в новизне, а в том, как они смогли себя проявить уже в XXI веке. Рассказываем, для чего сегодняшним лауреатам пришло в голову их использовать и как это поможет избежать медицинских трагедий.
На рубеже 1950-х и 60-х годов тысячи европейских детей появились на свет с тяжелыми пороками развития. У кого-то был недоразвит пищевод или мочевой пузырь, другим не хватало ушных раковин, третьим — пальцев, локтей или голеней, а то и целых конечностей. Такие аномалии встречались особенно часто у тех, чьи матери в первый месяц беременности принимали талидомид — успокоительное средство, которое незадолго до этого вышло на рынок. А через полтора десятка лет выяснилось, что проблема не в принципе действия лекарства — а в том, что около трети молекул действующего вещества в каждой его таблетке были не той формы.
Злое отражение
Талидомид — одна из тех молекул, у которых зеркальное отражение не совпадает с ними самими (их называют хиральными). Состав у них одинаковый, но некоторые свойства — разные. В хиральности талидомида виноват один из атомов углерода, который входит в его состав. Этот углерод образует четыре одинарные связи, и все — с разными химическими группами. А у его зеркального отражения эти группы расположены в другой последовательности — как пальцы на правой и левой руках, которые одинаковы по строению, но следуют друг за другом в разном порядке.
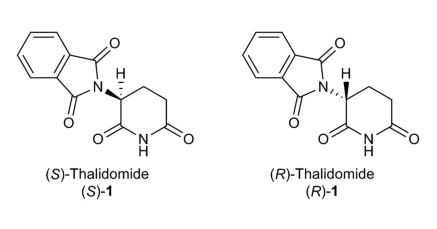
Справа лекарство R-талидомид, слева его зеркальное отражение, токсин S-талидомид
Etsuko Tokunaga et al. / Scientific Reports, 2018
Смесь из двух вариантов талидомида получается естественным образом на производстве. Но в 1950-х годах никто не позаботился о том, чтобы ее разделить. А зря. Технически, зеркально отраженные молекулы талидомида (их называют оптическими изомерами или энантиомерами) — это то же самое вещество: идентичные наборы атомов объединены в одни и те же группы одними и теми же связями. Но из-за того, что у них разная форма, для клетки это две принципиально разные молекулы. Подобно тому, как левшам неудобно браться за ножницы, рассчитанные на правшей, клеточные белки по-разному связываются с «правыми» и «левыми» изомерами (их называют D- и L-) одного и того же вещества. В некоторых случаях это приводит к тому, что лекарство просто становится бесполезным. В случае с талидомидом оно превратилось в яд (другие примеры такого рода можно найти в нашем тесте «Убийца из зазеркалья»).
Через пять лет после выхода на рынок талидомид оказался под запретом в большинстве стран — а ученые остались разбираться с последствиями. Одни занялись подробным изучением его свойств (и впоследствии нашли способ применить его против рака и лепры), другие обновили стандарты клинических испытаний: теперь каждый препарат разработчики обязаны проверить на млекопитающих, причем на представителях нескольких отрядов, прежде чем давать его людям.
А химики взялись придумать, как сделать так, чтобы этого больше не повторилось. «Когда-то раньше, несколько десятилетий тому назад, лекарственные препараты можно было в такой энантиомерно нечистой форме применять — вспоминает в разговоре с N + 1 Валентин Анаников, заведующий лабораторией металлокомплексных и наноразмерных катализаторов Института органической химии РАН, — но это давно закончилось. После истории с талидомидом и еще пары не таких громких историй все лекарственные препараты должны быть хирально чистыми». Иными словами, нужно любой ценой добиваться того, чтобы при синтезе вещества получался только нужный изомер, а не его зеркальный двойник.
Надзор за формой
В живой природе контролем за хиральной чистотой обычно занимаются ферменты — поскольку именно они отвечают за превращения биологических молекул. Для того, чтобы ускорить, то есть катализировать эти превращения, ферментам служит активный центр — это карман сложной формы, в который заходят участники реакции. Собирая их вместе, фермент подталкивает вещества к тому, чтобы те вступили во взаимодействие, — в тесноте вероятность этого гораздо выше, чем если бы они просто плавали рядом в растворе. А в результате этого тесного взаимодействия образуется всегда один и тот же энантиомер.
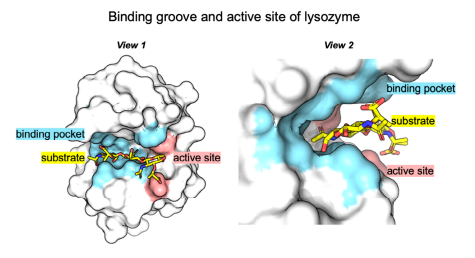
Фермент лизоцим и его активный центр
Ratul Chowdhury et al. / AlChe Journal, 2019
Но использовать ферменты для синтеза лекарств очень непросто. Во-первых, они привыкли жить внутри клетки и не всегда соглашаются работать, например, при высоких температурах, которые бывают нужны для синтеза органических веществ в промышленном «котле». Во-вторых, их самих довольно сложно раздобыть — для этого приходится строить инкубаторы, заселять их генетически модифицированными клетками и ждать, пока они нарастят нужное количество фермента.
Еще больше времени может занять поиск фермента под конкретную реакцию. В природе никакого талидомида не существует, как не существует и многих других нужных людям лекарств — а значит, может не найтись и фермента, который смог бы их синтезировать. Приходится либо искать похожие реакции в клеточном обмене веществ, либо заставлять ферменты эволюционировать и надеяться, что они сделают это в нужном нам направлении (за метод направленной эволюции Нобелевскую премию по химии вручили в 2018 году, об этом наш текст «Игра в бога»).
Поэтому фармкомпаниям вместо капризных ферментов катализаторами, как правило, служат атомы металлов. Они могут объединяться в комплексы с органическими молекулами, умеют отдавать и принимать электроны, чем активируют участников реакции и побуждают их вступить во взаимодействие, чтобы восстановить электронный баланс. Но атомы металлов слишком малы и слишком симметричны, чтобы развернуть молекулу нужной стороной, — а значит, не способны проконтролировать хиральность продукта. На выходе получается смесь энантиомеров, которые нужно разделять, что тоже довольно сложно и затратно.
Эту проблему решили лауреаты Нобелевской премии по химии, которую вручили 20 лет назад: Уильям Ноулз, Рёдзи Ноёри и Барри Шарплесс. Они научились делать катализаторы из асимметричных органических молекул, соединенных с атомом металла: таким образом на выходе образовывался нужный энантиомер. Их разработки быстро нашли применение в фармацевтической промышленности, благодаря им удалось наладить производство леводопы — лекарства от паркинсонизма, в основе которого лежит L-аминокислота фенилаланин.
Но применение этой технологии не обходится без издержек для производителя: после того, как реакция закончилась и образовался продукт, смесь нужно очистить. «Очень много сложных лекарственных препаратов делается с катализом на палладии, — говорит Анаников, — это тяжелый металл, его примеси остаются [в препарате]. Естественно, никто не хочет покупать таблетки с палладием, это добром не кончится, поэтому надо чистить. А это очень дорого и тяжело».
Разбирая фермент
За пару лет до того, как Ноулз, Ноёри и Шарп получили свое приглашение на церемонию вручения Нобелевской премии, молодой биохимик Беньямин Лист решил выяснить, каким именно инструментом пользуются ферменты для контроля хиральности — вдруг получится у них его позаимствовать? Основная задача любого асимметрического катализатора — перенести информацию о хиральности на целевую молекулу. На первый взгляд, каталитическая способность ферментов должна полностью определяться тем, как устроены их активные центры.
Свои наблюдения ученый начал с фермента альдолазы и реакции, которую она катализирует: «пришивает» к ацетону ароматический альдегид. В качестве промежуточной стадии при этом образуется енамин, в котором атом азота находится рядом с двойной углерод-углеродной связью, а соседний с ним атом углерода — хиральный. Лист уже знал, как устроен активный центр альдолазы, и знал, что за образование енамина отвечает аминокислота L-пролин. Осталось понять, будет ли ее одной достаточно для катализа.
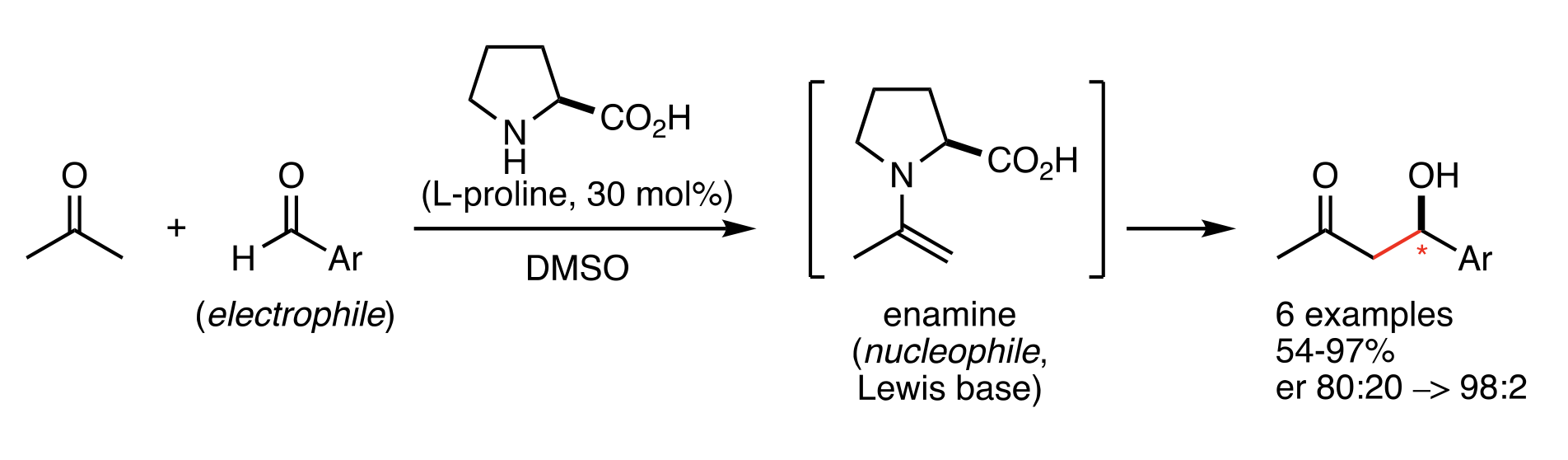
Реакция альдольной конденсации, для которой Лист искал хирализующий катализатор
Nobel Prize
«Конечно, там были сложности, — говорит Денис Чусов, старший научный сотрудник Института элементов органических соединений РАН. — Потому что аминокислоты не очень хотят растворяться в органических растворителях. А в воде такие реакции проводить очень сложно: там тончайшие эффекты, которые вода, конечно, разобьет. Но когда получилось, он, конечно, сразу понял, что у него в руках и какое это открытие».
В другом растворителе, диметилсульфоксиде, Листу действительно удалось использовать хирально чистый L-пролин как катализатор — и сделать из нехиральных альдегида и кетона хирально чистый альдоль.
Получилось, что огромная молекула фермента и сложная геометрия активного центра совсем не обязательны, чтобы получить хирально чистый продукт. Для этого достаточно одной маленькой хирально чистой молекулы, которая будет образует промежуточный комплекс и делает катализ асимметрическим.
Хирализуя катализатор
В то же самое время Дэвид Макмиллан шел к похожей идее совсем с другой стороны. Он пытался позаимствовать принцип работы не у ферментов, а у маленьких молекул, известных катализаторов, которые на на промежуточной стадии образуют временные комплексы с одним из реагентов.
Один из таких катализаторов, который часто используют и в промышленности, — это кислота Льюиса (например, AlCl3). Ни о какой хиральности применительно к хлориду алюминия говорить нельзя. Поэтому Макмиллан задался целью найти для кислоты Льюиса органический хиральный аналог.
В качестве модельной реакции Макмиллан его коллеги взяли реакцию Дильса — Альдера — присоединения к диену соединения с двойной связью. В качестве реагентов Макмиллан взял циклопентадиен и α,β-ненасыщенный альдегид.
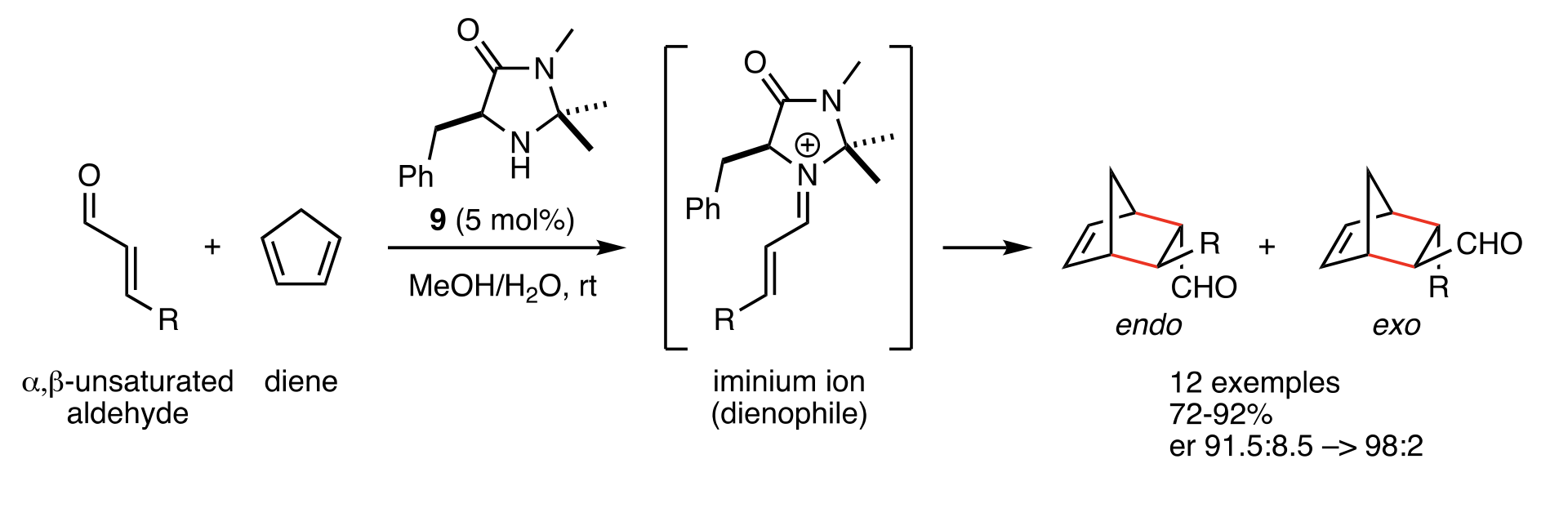
Реакция Дильса — Альдера, для которой Макмиллан искал хирализующий катализатор
Nobel Prize
В результате такой реакции образуется бициклическое соединение, в котором к соседним атомам углерода напротив двойной связи присоединены альдегидная группа и радикал с противоположного хвоста альдегида. В зависимости от того, как эти группы развернуты относительно мостика бицикла, может получиться два различных энантиомера.
В качестве катализатора Макмиллан решил использовать циклический вторичный амин. Такой катализатор цепляется к альдегиду — получается иминий, ион, в котором положительно заряженный атом азота соединен двойной связью с одним из соседних атомов углерода. Ключевая идея работы Макмиллана — в том, что на промежуточном этапе такой реакции образуется хиральный комплекс, что приводит к асимметрии реакции.
Фактически Макмиллан пришел к тому же выводу, что и Лист: если в каталитической реакции образуется промежуточный комплекс с хирально чистым катализатором, то из нехиральных реагентов можно получить хирально чистый продукт. Но пришел к этой идее, вводя хиральность в известный механизм катализа.
Почти одновременно
Макмиллан отправил свою статью в журнал в январе 2000 года. В ней впервые появляется слово «органокатализ» — ученый тем самым подчеркивал, что не так важно, какую именно молекулу он сделал катализатором. По его мнению, гораздо важнее был сам принцип — что хиральная органическая молекула может передавать хиральность «по наследству» продуктам реакции, которую катализирует.
В этом отдельная ценность «нобелевских» статей Листа и Макмиллана. Ученым не всегда удается сформулировать сразу, почему феномен, открытый ими экспериментально, вообще так работает. Например, с предыдущей премией за асимметрический катализ, 2001 года, все было не так. «Реакцию нашли в 50-х годах еще, — вспоминает Чусов, — а механизм предложили только в 70-х. То есть люди использовали реакцию, заводы построили уже, применяли, но как это работает — совершенно непонятно было. А тут — когда [Лист и Макмиллан] нашли эту реакцию, они задумались, как это работает. И предложили очень простое объяснение — действительно, когда смотришь, то понимаешь, что так оно и должно быть».
Во введении к своей статье Макмиллан предсказал, что реакций, к которым можно применить обнаруженный им принцип, должно быть много — а значит, будет много и органических катализаторов. И тем самым предвосхитил статью Листа, которую даже опубликовали раньше, чем статья самого Макмиллана вышла в печать.
За следующие 20 лет органических катализаторов действительно стало больше. Многие фармкомпании уже зарегистрировали патенты на использование этого метода для создания самых разных лекарств: от повышенного давления и депрессии, воспаления и вирусного гепатита. Органический катализ мог бы сделать производство гораздо выгоднее и быстрее: например, синтез популярного лекарства от гриппа он ускорил в целых 30 раз. Правда, пока сложно сказать, насколько компании действительно пользуются этим методом. «Ученые, которые занимаются формально фундаментальной наукой, возможно прикладной — они не знают, что использует промышленность, — рассказывает Чусов. — Потому что промышленность стремится не раскрывать детали. Но общаясь с людьми, которые возглавляли R&D фармацевтических гигантов, я могу сказать, что в первую очередь они проверяют разработку Листа, по той причине, что это дешево, очень безопасно, и это можно мешками использовать».
Не прекратили своих исследований и Макмиллан с Листом. Например, Макмиллан соединил асимметрический органокатализ с окислительно-восстановительным фотокатализом. В результате получилась система, похожая на фотосинтез у растений — она преобразуют солнечный свет в химическую энергию. А Лист приспособил для катализа другие аминокислоты, хотя пролин до сих остается его любимцем: «Кстати, сладковатый на вкус, — поделился сегодня утром ученый, говоря об этом с журналистами, — как мое тогдашнее открытие».
О своей Нобелевской премии отцы органокатализа тоже узнали почти одновременно, правда, по-разному. Макмиллан рассказал журналистам, что получил от «кого-то из Стокгольма» сообщение, в котором его имя было написано с ошибкой. Он подумал, что это пранк от кого-то из его бывших коллабораторов, и лег обратно спать. Чуть позже с ним связался Лист, чтобы поделиться радостными новостями — но Макмиллан снова не поверил. Он поспорил с Листом на тысячу долларов, что немца разыграл тот же самый пранкер, и снова попробовал уснуть. Проснулся он уже от разрывающегося от поздравлений телефона — и узнал, что тысячу долларов придется отдавать.
Лист, кстати, тоже сегодня стал должником — правда, на сумму поменьше. «Когда я к нему ехал, — вспоминает Чусов, который сотрудничал с Листом несколько лет — я уже понимал, что он натворил в науке и что Нобелевская премия ему обеспечена. А он не очень верил. Мы с ним заключили пари, что в ближайшие 20 лет ему дадут премию. [Не знаю], вспомнит ли он, — смеется ученый, — но вообще спорили мы на 100 евро!»
Полина Лосева, Александр Дубов
Отправьте нам запрос
Поиск на сайте
Наши клиенты и партнеры
Недавние публикации
- В скелете вымершего псового с патагонского погребения заподозрили останки питомца индейцев 16 апреля 2024
- Что нужно для развития в России технологий ИИ, обсудили на форуме «Открытые инновации» 16 апреля 2024
- На снимках солнечного затмения заметили огромное розовое пламя 15 апреля 2024
- Найден источник крупнейшей после Большого взрыва вспышки в космосе 12 апреля 2024
- Формирование визуомоторных ассоциаций оказалось зависимо от мозжечка 12 апреля 2024
